العلاج الجديد لمرض الخلايا المنجلية: نقاش ومخاوف محدودة


لجنة من المستشارين أبدت بعض القلق خلال اجتماع عُقد يوم الثلاثاء الماضي مع إدارة الغذاء والدواء الأميركية، حيث تم مناقشة المخاطر المحتملة المتعلقة بعلاج جديد مُقرر استخدامه لعلاج مرض فقر الدم المنجلي باستخدام تقنية تحرير الجينات المعروفة بـ “كريسبر” (CRISPR). هذه المعلومات مأخوذة من تقرير نُشر على موقع أخبار “سي بي إس”.
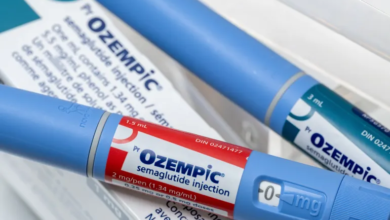
إذا تمت الموافقة عليه من قبل إدارة الغذاء والدواء الأميركية، سيصبح العلاج المسمى “إيكسا-سل” (exa-cel)، الذي تنتجه شركة “فيرتيكس فارما سوتيكال”، أول علاج متاح للعديد من المرضى الذين يعانون من هذا النوع من فقر الدم.
من المقرر أن تصدر إدارة الغذاء والدواء الأميركية قرارًا بشأن الموافقة على “إيكسا-سل” بحلول الثامن من ديسمبر/كانون الأول القادم، وفقًا لبيان صحفي نُشر من قبل شركة فيرتيكس.
كيف يعمل العلاج الجديد؟
علاج “إيكسا-سل” يعتمد على جمع الخلايا الجذعية من المريض، وباستخدام تقنية الكريسبر، يقوم الأطباء بتعديل هذه الخلايا لإصلاح المشاكل الوراثية التي تُسبب مشكلة الخلايا المنجلية. بعد ذلك، يتم إعادة الخلايا الجذعية المعدلة إلى المريض في حقنة واحدة.
ما هي تقنية كريسبر؟
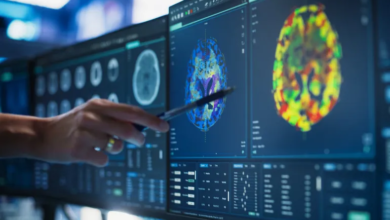
تقنية “كريسبر” (CRISPR) هي وسيلة لتعديل الجينات تسمح بتعديل الحمض النووي للكائنات الحية، بما في ذلك الإنسان. يهدف العلماء إلى استخدامها في علاج الأمراض.
تتميز تقنية “كريسبر” بأنها تعتبر منخفضة التكلفة وسهلة الاستخدام، وتسمح للباحثين بتعديل الجينات باستخدام ما يشبه “مقصًا” جينيًا يشبه في وظيفته برامج معالجة النصوص. يمكن لهذا المقص تتبع واكتشاف الأخطاء الجينية وإصلاحها بواسطة تدخلات أخرى في الحمض النووي.
تعتمد تقنية “كريسبر” على إنزيم يُسمى “كاس 9” (Cas9)، الذي يستخدم جزيئًا موجهًا من الحمض النووي الريبي لاستهداف الجزء المعني من الحمض النووي. ثم يقوم بتعديل الحمض النووي لفك تشفير الجينات أو إدخال تسلسلات جينية محددة.
ماهو مرض فقر الدم المنجلي؟
مرض فقر الدم المنجلي هو مجموعة من الاضطرابات الوراثية التي تؤثر على خلايا الدم الحمراء، مما ينجم عنه مشكلة في هيموغلوبين الدم. وفقًا لموقع ميدلاين بلاس التابع للمكتبة الوطنية للصحة في الولايات المتحدة الأمريكية.
الهيموغلوبين هو بروتين موجود في خلايا الدم الحمراء ويقوم بنقل الأكسجين في جسم الإنسان. في حالة فقر الدم المنجلي، يتكون الهيموغلوبين على شكل “قضبان صلبة” داخل خلايا الدم الحمراء، مما يغير شكلها الطبيعي. بدلاً من أن تكون هذه الخلايا على شكل أقراص، تصبح على شكل هلال أو منجل.
خلايا الدم المنجلية ليست مرنة ولا يمكنها تغيير شكلها بسهولة، وتنفجر العديد منها أثناء تحركها في الأوعية الدموية. عادةً ما تعيش هذه الخلايا لمدة قصيرة تتراوح بين 10 و 20 يومًا فقط، بدلاً من 90 إلى 120 يومًا كما هو الحال في الخلايا الدم الحمراء الطبيعية.
نتيجة لهذا التدمير المبكر للخلايا المنجلية، يصبح الجسم غالبًا غير قادر على إنتاج ما يكفي من الخلايا الدم الحمراء لتعويض الخسائر. هذا يؤدي إلى حالة تُعرف باسم فقر الدم، والتي قد تتسبب في التعب والإجهاد للشخص المصاب.
بالإضافة إلى ذلك، يمكن للخلايا المنجلية أن تلتصق بجدران الأوعية الدموية، مما يمكن أن يؤدي إلى انسداد الأوعية وتقليل تدفق الدم أو إيقافه تمامًا. في مثل هذه الحالات، يصعب على الأكسجين الوصول إلى الأنسجة المجاورة، مما يمكن أن يتسبب في حدوث نوبات مفاجئة وشديدة من الألم، والتي قد تتطلب العناية الطبية الفورية في المستشفى.
ما سبب مرض فقر الدم المنجلي؟
سبب مرض فقر الدم المنجلي هو وجود جين معيب يُعرف باسم جين الخلية المنجلي. يتم ولادة الأشخاص المصابين بالمرض عندما يرثون جينين من الخلايا المنجلية، وذلك من كل من والديهم.
إذا وُلد الفرد بجين واحد من الخلايا المنجلية، يُطلق عليهم عادة اسم “سمة الخلية المنجلية”. يكون الأشخاص الذين يحملون سمة الخلية المنجلية عادة في صحة جيدة عمومًا، ولكن لديهم القدرة على نقل الجين المعيب إلى أبنائهم.
وتشير المعاهد الوطنية للصحة في الولايات المتحدة إلى أن الخيار الوحيد حاليًا لعلاج مرض فقر الدم المنجلي هو إجراء زرع نخاع العظم أو زرع الدم، والتي تكون متاحة لنسبة صغيرة من المرضى الذين يمكنهم العثور على متبرعين يتطابقون جينيًا معهم.
حياة أقصر بكثير
أعلنت إدارة الغذاء والدواء الأميركية للجنة أن البالغين الذين يعانون من مرض فقر الدم المنجلي يمكن أن يعيشوا الآن حياة أطول بفضل التقدم الطبي، لكن من المرجح أن تكون هذه الحياة “أقصر بكثير” من المتوقع.
أثبتت التجارب على علاج “إكسا-سيل” نجاحًا ملموسًا ومُشجعًا ووصفته شركة فيرتكس بأنه “غير مسبوق” بالنسبة للمرضى الذين يعانون من مرض فقر الدم المنجلي الحاد. هذا النجاح أدى إلى تقليل حالات دخول المستشفى بسبب أزمات انسداد الأوعية الدموية بشكل كبير لدى المرضى الذين تلقوا جرعة واحدة من إكسا-سيل.
ووفقًا للوثائق التي تم نشرها قبل اجتماع أمس الثلاثاء، أبدت إدارة الغذاء والدواء الأميركية تأييدها الكبير للبيانات التي قدّمتها الشركة بشأن “النتائج الإيجابية البارزة” التي تم تحقيقها في تجارب العلاج.
وفي الاجتماع، أشارت الدكتورة نيكول فردان، رئيسة مكتب المنتجات العلاجية التابع لإدارة الغذاء والدواء الأميركية، إلى أن “تمت دراسة إكسا-سيل بعناية كبيرة لعلاج مرض فقر الدم المنجلي مع أزمات انسداد الأوعية الدموية الشديدة وقد أظهرت فعاليتها”.
لم تُطلب من اللجنة الاستشارية للعلاجات الخلوية والأنسجة والجينات التصويت على توازن الفوائد والمخاطر المقدمة من “إكسا-سل”، وهو ما عادة ما تطلبه الوكالة عند تقييم قرارات الموافقة الصعبة. بدلاً من ذلك، طُلب من مسؤولي إدارة الغذاء والدواء التركيز فقط على مناقشة المخاوف من أن شركة فيرتيكس قد تحتاج إلى مزيد من الجهد لدراسة احتمال أن تؤدي تقنيتها في حالات نادرة إلى تغيير أجزاء أخرى من الجينوم عن طريق الخطأ.
قال كومودي سينغ من إدارة الغذاء والدواء الأميركية: “إذا كان الجين يلعب دورًا أساسيًا في وظيفة الخلية، فإن مثل هذه التعديلات غير المقصودة يمكن أن تكون ضارة. ويمكن أيضًا أن تزيد من خطر الإصابة بالسرطان.”
في العروض التقديمية التي قدمتها شركة فيرتيكس إلى اللجنة، أكدت الشركة أنها اتبعت عدة استراتيجيات لتقليل مخاطر التحرير الجيني غير المقصود وفحص المسارات المحتملة التي يمكن أن تؤدي إلى التعديلات غير المقصودة. وأشارت الشركة إلى أن الخلايا التي تتعرض لتقنية كريسبر تتعرض لها لفترة قصيرة فقط بعد سحب الدم من المرضى، وذلك قبل إعادة حقنها مرة أخرى في المرضى.
وأعترف الخبراء الذين قدموا إلى اللجنة أيضًا بالمخاوف النظرية من أن التعديلات غير المستهدفة قد تسبب سرطان الدم. ومع ذلك، فإن العديد من التغييرات غير المقصودة قد لا تكون لها تأثير على المرضى. أعرب أعضاء اللجنة إلى حد كبير عن دعمهم لهذا العلاج، بالإضافة إلى دعم بعض الإجراءات الإضافية بعد إطلاقه لدراسة مخاطره على المدى الطويل.